同病異治: 次世代基因定序檢測 NGS 之精準治療
隨著分子生物學與基因體學的迅速發展,醫學研究走向從細胞的的層次來找出疾病發生的根本原因。在臨床上,傳統以病理型態為基礎的「同病同治」模式正逐漸被「同病異治」的新思維所取代,即同為相同診斷的癌症,患者間的基因突變、表觀調控與免疫微環境仍存在顯著差異,導致對藥物反應與預後的多樣化。近年來,次世代基因定序(Next Generation Sequencing, NGS) 技術的應用,使臨床醫師得以在單一檢測中解析數百至上千個與癌症相關的基因,找出潛在的驅動突變(driver mutation)與可藥靶標(actionable targets),進而依據分子特徵設計個別化治療策略。這種以基因異質性為導向的「精準治療(precision oncology)」不僅提升治療反應率與生存效益,也避免了傳統治療的盲目性與副作用負擔。
次世代基因定序(Next Generation Sequencing, NGS)是什麼 ?
在了解基因定序之前,先介紹一下次世代基因定序(Next Generation Sequencing, NGS)原理。簡單來說,就是將DNA (也可以是RNA) 打碎成數百萬個約 200個鹼基長度的小片段,然後使之附著在特殊的載體或晶片上進行擴增。擴增的過程中,利用螢光訊號或電子訊號變化而得知序列。之後得到數以億計的序列片段數據。最後利用電腦程式將這些片段拼組起來,並且與資料庫內的基因序列進行比對,而得以知道突變的位點與比例。
依據對基因體解析的程度,又可以分成全外顯子定序(whole exome sequencing, WES)及全基因定序(whole genome sequencing, WGS)。前者是只針對可以轉譯出蛋白質的基因序列來,後者是定序整個基因體的序列,包括眾多的非編碼DNA (Non-coding DNA)。接下來的問題是: 在治療病人的醫療現場上,我們需要知道所有的基因編碼嗎? 目前顯然是不需要,人類約有2萬個基因,還有許多未探明的區域,目前已知跟癌症相關的基因是相對少數。
全方位基因體分析(Comprehensive Genomic Profiling, CGP) 與 目標基因定序 / 標靶基因定序 (Targeted-Panel Sequencing, TPS)
現行臨床上或市面上應用於癌症基因檢測的項目稱作全方位基因體分析(Comprehensive Genomic Profiling, CGP)。這個中文譯名很容易讓人誤以為是分析癌症組織中完整的基因體,實際上不然,它只針對數百個與癌症相關的基因以及關鍵生物標誌進行高深度定序分析,換句話說無法應用在癌症之外的疾病(例如神經退化性疾病)。目標基因定序 / 標靶基因定序 (Targeted-Panel Sequencing, TPS),則更侷限針對特定癌種或明確靶點進行檢測。目前臨床可用的 CGP 或 TPS 檢測已有多種商業化產品,多數為引進自國外且經臨床驗證或監管機構認可(如 FDA 或 CE-IVD)的檢測平台,供醫院與生技公司提供臨床檢測服務。
台灣在精準醫療檢測的推行上,其實存在某種程度的「名不符實」。依照現行法規,凡醫院實驗室或生技公司欲提供基因檢測服務,皆須通過衛生福利部對「實驗室開發檢測(Laboratory Developed Tests, LDTs)」的審查。從字面上看,LDT 應指由各實驗室或公司自行設計與開發的檢測方法;然而實際情況卻並非如此。據筆者了解,目前台灣多數提供基因檢測服務的單位,其檢測內容多為引進國外已獲認證並商業化的全方位基因體分析(Comprehensive Genomic Profiling, CGP)產品,真正由本土團隊自行開發、驗證與建立流程的案例反而相對少數。不過由於NGS操作過程需要更精細與分析的技術門檻較高,更嚴謹的專業品質認證有其必要性。
癌症基因檢測的應用
癌症的基因檢測在臨床醫療上的應用,主要涵蓋診斷輔助、治療指引、預後評估以及治療反應監測等面向。在部分診斷困難或組織來源不明的腫瘤中,基因檢測結果往往能提供關鍵線索,協助釐清腫瘤來源與性質。
筆者曾遇過一個印象深刻的病例:患者初步診斷為胰臟癌侵犯十二指腸,病理切片顯示為分化極差的腺癌,在形態學上難以確定原發部位。後續進行次世代基因定序(NGS)後,意外發現該腫瘤帶有 EGFR L858R 突變——這是肺腺癌最常見的驅動基因變異之一。相對地,約九成以上的胰臟腺癌具有 KRAS 突變,而本例中 KRAS 基因竟為野生型(wild-type)。這項基因特徵的對比最終提示,該病例極可能是肺癌轉移至胰臟及十二指腸,而非原發性胰臟癌。後續病患接受非小細胞肺癌的標靶藥物治療,效果良好。
隨著定序技術的進步,現今我們已能透過 NGS 技術分析血液中的游離核酸(circulating free DNA, cfDNA)或循環腫瘤細胞(circulating tumor cells, CTCs)。這項被稱為液態生檢(liquid biopsy)的技術,能在無需侵入性取樣的情況下,偵測體內腫瘤相關的基因變異。藉此,我們可動態追蹤病患對治療的反應,並在尚未出現異常前,提前偵測微量殘存疾病(minimal residual disease, MRD)或疾病復發的跡象。
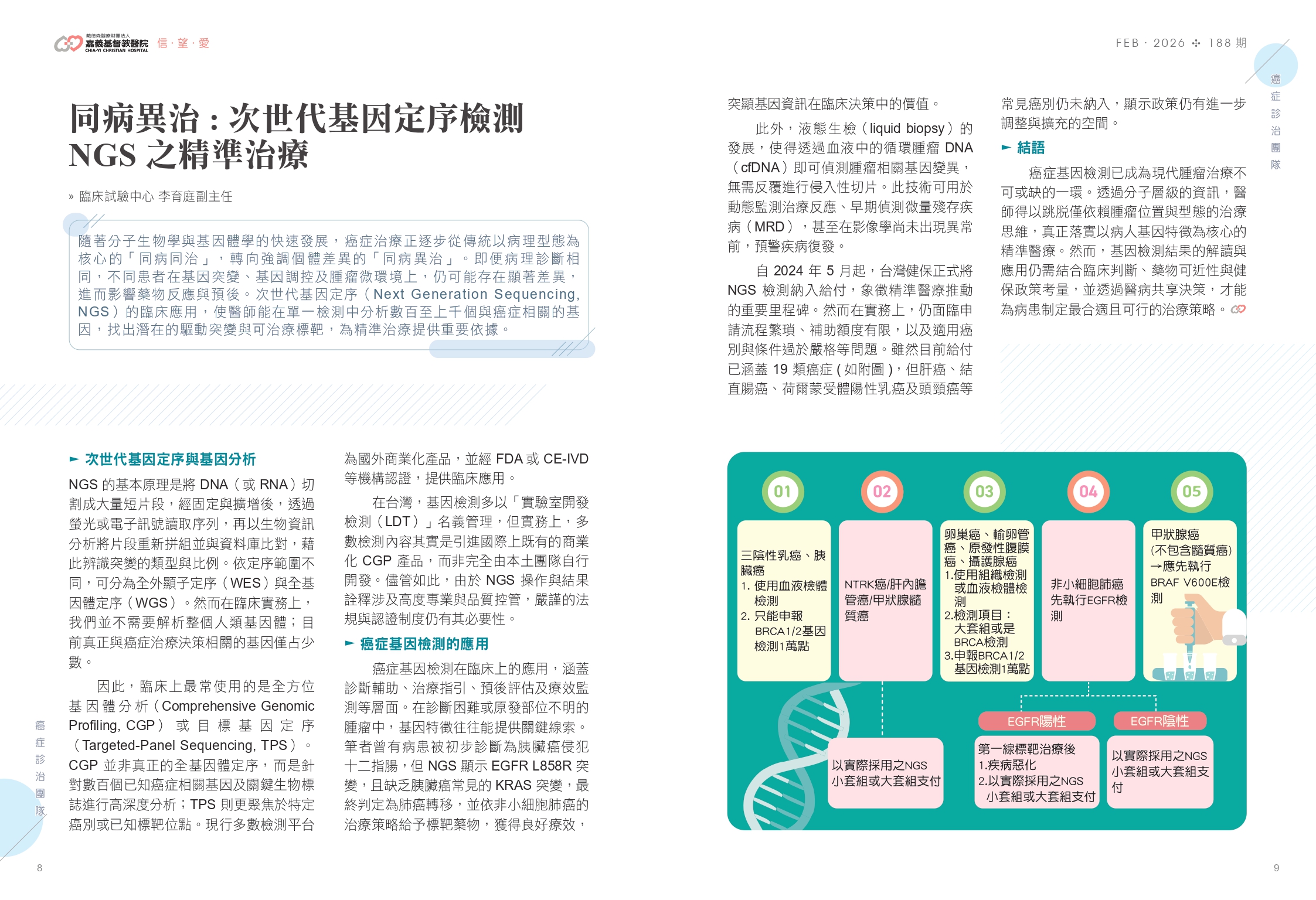
自 2024 年 5 月 1 日起,健保正式將 次世代基因定序(NGS)檢測 納入給付範圍,這無疑是推動國內精準醫療發展的重要里程碑。然而在實務運作上,筆者仍不免感到有些「為德不卒」。主要困境包括:繁瑣且不便的申請流程、補助額度有限,以及病人適用條件依伴生診斷項目為主且過於嚴格(如圖所示)等多重因素,導致政策效益未能完全落實。儘管目前給付已涵蓋 19 類癌症,實際上仍有多數常見癌別未被納入。例如台灣盛行的 肝癌、結直腸癌、荷爾蒙受體陽性的乳癌 及 頭頸癌 等,目前皆不在健保給付名單內。此一現況使得部分臨床上具明確分子標靶需求的病患,仍須自費進行檢測,反映出台灣在精準醫療政策推行上仍有進一步優化與擴充的空間。
癌症基因檢測已成為現代癌症治療中不可或缺的重要一環。透過基因體層級的資訊,我們得以深入了解腫瘤的分子機制,找出驅動疾病的關鍵變異,並據以制定個別化的治療策略。這正是精準醫療(Precision Medicine)的核心精神——以病人的基因特徵而非僅以腫瘤位置為依據,選擇最適切的治療方式。
然而,基因檢測與臨床應用之間仍涉及多層次的解讀與決策,包括結果詮釋、藥物可近性、健保政策與倫理議題等。因此,最適當的做法仍是與主治醫師及專業團隊充分討論,根據病患的臨床狀況與分子特徵,共同研擬出最符合個別需求的治療策略。